乳液聚合技术作为获取高聚物的重要方法之一,它起始于20 世纪初,并于30 年代开始广泛工业化。目前,乳液聚合大多分为常规水包油型乳液聚合、反相的油包水型乳液聚合、介于溶液聚合与乳液聚合之间的多相乳液聚合、以液氨、甲酰胺、甲酸等为分散介质的非水分散介质乳液聚合、有机分散介质分散乳液聚合、辐射乳液聚合、无胶束乳液聚合、双连续乳液聚合、乳液定向聚合、杂化乳液聚合、原子转移自由基乳液聚合等,它们的影响因素各有异同,本文将对常规乳液聚合的影响因素进行讨论。常规乳液聚合就是以油相为分散相,水为连续相的水包油型乳液聚合。虽然常规乳液聚合最简单的配方只是由单体、水、水溶性引发剂和乳化剂4部分组成,但其体系具有特定的复杂性,影响因素很多,以下将对单体、乳化剂、引发剂、缓冲剂、温度、搅拌速率和聚合工艺等因素进行介绍。
1 单体
1.1 主要单体
能进行乳液聚合的单体种类很多,在常规乳液聚合中应用得比较广泛的有乙烯基单体、共轭二烯单体、丙烯酸及甲基丙烯酸系单体。这些单体在乳液聚合中作为主要单体,它们在水中溶解度很小,与水的表面张力相差很大,在静置时分为两层。加入乳化剂后由于单体可以进入胶束内,单体在乳化剂溶液中的溶解度增加,单体就可以稳定地分散在体系中,形成水包油体系,混合单体的乳化稳定性与乳液共聚稳定性结果一致。如要乳液聚合顺利进行,单体还必须符合以下3 个条件:(1)可以增溶溶解但不是全部溶解于乳化剂水溶液;(2)可在增溶的温度下进行聚合;(3)与水或乳化剂无任何活化作用,即不水解。作为乳液聚合的反应物,单体与水的比例可在很宽的范围内波动,一般单体占整个乳液聚合配方的30%~60%。当分散相体积分数达到74%(同样大小的乳胶粒紧密堆积在一起时,分散相所占的体积分数为74%)的乳液称为超浓乳液,已不属于常规乳液聚合的范畴。
1.2 功能单体
单独由上述单体得到的聚合物乳液在实际应用中愈来愈暴露出不足,因此常规乳液聚合中功能单体经常配合主要单体一同使用。根据特殊的需要添加不同官能团的单体,制得的乳液既具有主单体聚合物的性能,又能达到其他方面的效果,如增加乳液成膜后的弹性、刚性、附着力、耐水性、耐热性、耐候性等。这些功能单体一般带有极性基团,如羧基、羟基、氨基、酰胺基及缩水甘油基等,它们之间既能够自交联也能相互交联,而且对水的亲和力较大,在一定程度上起到辅助乳化剂的作用。适量地加入可以使共聚物产生轻微的交联,形成一定程度的网络结构,把聚合物分子链间的分子作用力转变为化学键,提高共聚物的刚性,而且亲水极性基团的引入降低了乳胶粒与水的界面能,稳定了聚合过程,减少絮凝的生成。其加入量约为主单体的2%~6%,过低则起不到改性效果或改性不明显,过高会令聚合体系中交联点增多,乳液粘度上升,散热困难,自升温程度加大,使共聚体系凝聚而失稳,涂膜的耐水性反而下降。
2 乳化剂
2.1 乳化剂的作用
乳化剂是可以形成胶束的一类物质,分子中同时存在亲水基团和亲油基团,是乳液聚合系统中的关键组分之一。在通常情况下,乳化剂并不参加化学反应,但其在乳液聚合过程中起着举足轻重的作用。在常规乳液聚合中,其主要作用是:降低水的表面张力、降低油水界面张力、增溶单体、乳化单体以及分散稳定聚合物。反应前在水中加入乳化剂后,乳化剂的亲水基团溶于水,亲油基团却被水推开,指向空气,部分或全部水面被亲油基团覆盖,将部分水- 空气界面变成亲油基团- 空气界面,油的表面张力小于水,所以乳化剂水溶液的表面张力,即在乳液聚合体系中水相的表面张力小于纯水的表面张力。
在水中加入单体后,单体和水不互溶,单体呈油相存在,油和水的界面张力很大,仅仅通过搅拌不能形成稳定的乳液体系,最终只会相分离。这时体系中乳化剂的亲油基团必定指向油相,而亲水基团则在水中。这样在油水相界面的油相一侧附着了一层乳化剂分子的亲油端,将部分或全部油-水界面变成亲油基团-油界面,降低了界面张力。另外,当乳化剂加到一定浓度时,乳化剂以胶束的形式存在。通过搅拌,单体形成许多珠滴,然后被增溶溶解在乳化剂胶束内,表面吸附了一层乳化剂,乳化剂的亲油基团,也就是胶束中与单体结构相似的烃基部分,伸向单体珠滴内部,亲水基团则露在水相。单体珠滴之间存在静电斥力,难于聚结成大珠滴,形成稳定的乳状液体系,为聚合过程提供引发场所——单体增溶胶束。
在水中加入单体后,单体和水不互溶,单体呈油相存在,油和水的界面张力很大,仅仅通过搅拌不能形成稳定的乳液体系,最终只会相分离。这时体系中乳化剂的亲油基团必定指向油相,而亲水基团则在水中。这样在油水相界面的油相一侧附着了一层乳化剂分子的亲油端,将部分或全部油-水界面变成亲油基团-油界面,降低了界面张力。另外,当乳化剂加到一定浓度时,乳化剂以胶束的形式存在。通过搅拌,单体形成许多珠滴,然后被增溶溶解在乳化剂胶束内,表面吸附了一层乳化剂,乳化剂的亲油基团,也就是胶束中与单体结构相似的烃基部分,伸向单体珠滴内部,亲水基团则露在水相。单体珠滴之间存在静电斥力,难于聚结成大珠滴,形成稳定的乳状液体系,为聚合过程提供引发场所——单体增溶胶束。
随着聚合反应的进行,单体聚合成聚合物小颗粒。体系变为聚合物小颗粒、单体珠滴、乳胶粒和水的混合物。由于比重的不同及颗粒的相互粘结作用,不能形成稳定的分散体系。乳化剂的存在令聚合物表面吸附上一层乳化剂分子,在每一个聚合物小颗粒上都带上一层同号电荷,因而它们都能稳定地分散并悬浮在介质中。正是由于乳化剂的这种分散作用保证了合成胶乳中的乳胶粒不凝聚,使乳液聚合得以顺利进行。
2.2 乳化剂的种类及影响
任何乳化剂都含有亲油基团和亲水基团,亲油基团就是乳化剂中的非极性部分,亲水基团就是乳化剂中的极性部分。根据亲水基团的不同,可将乳化剂分为4 类:阴离子型乳化剂、阳离子型乳化剂、非离子型乳化剂和两性乳化剂。
阴离子型乳化剂在水中发生解离,得到金属阳离子或铵根离子和含有亲油基团的亲水阴离子。在常规乳液聚合中使用的阴离子型乳化剂的亲油基团一般是C11~C17 的直链烷基或C3~C8 的烷基与苯基或萘基结合在一起组成的,与亲油基团相连的亲水基团为阴离子,如羧酸根离子,硫酸根离子,磺酸根离子和磷酸酯酸根离子。常用的阴离子型乳化剂有脂肪酸钠RCOONa(R=C11~C17),十二烷基硫酸钠C12H25OSO3Na,烷基磺酸钠RSO3Na(R=C12~C16),烷基芳基磺酸钠,如丁二基萘磺酸钠(C4H9)2C10H5SO3Na(俗称拉开粉),松香皂等。这些阴离子乳化剂具有较强的乳化能力,在碱溶液中比较稳定。但脂肪酸盐类乳化剂遇酸、钙离子、镁离子等会形成不溶于水的酸或金属皂,使乳化剂失效。在乳液聚合配方中需加pH 调节剂,如磷酸钠、碳酸氢钠、氨水等,保持溶液呈碱性,所用的水也必须不含与之形成不溶物的金属离子。硫酸盐类乳化剂及磺酸盐类乳化剂的乳化能力强,水溶性较大,比脂肪酸盐类稳定,适用范围宽,它们既可以在碱性条件下使用,又可以在酸性条件下使用,而且所制得的胶乳无论对酸还是对金属离子都具有较大的稳定性。在常规乳液聚合中当硫酸盐类乳化剂在烃链上有不饱和结构时,对聚合会有阻聚作用,使聚合速率减慢,且所制得的聚合物平均相对分子质量低,而采用烷基磺酸盐类乳化剂比相应的硫酸盐类乳化剂的聚合反应速率高,但所制得的聚合物相对分子质量低,磺酸盐烃链上的不饱和结构同样具有阻聚作用,对于烷基苯磺酸钠来说,当苯环上烷基链短时,必须具有两个以上烷基才能成为常规乳液聚合的有效乳化剂,磺酸盐类乳化剂的水溶性比硫
酸盐类差。
阳离子型乳化剂的极性基团为阳离子,如季铵盐类,可以用来制备带正电荷的乳液。虽然它不怕硬水并且耐酸,但由于其乳化能力稍差,还可能影响引发剂的分解,一般不被常规的乳液聚合所使用。
两性乳化剂分子中同时含有碱性基团和酸性基团,也就是亲水基团中同时兼有阴离子和阳离子,在酸性介质中可以离解成阳离子,在碱性介质中可离解成阴离子。这类乳化剂可分为羧酸型、硫酸酯型、磷酸酯型、磺酸型和氨基酸等。虽然该类乳化剂在任何pH 下都有效,但目前关于两性乳化剂的研究很少,应用于常规乳液聚合中鲜见。
非离子型乳化剂溶于水不能离解成正负离子,
非离子型乳化剂溶于水不能离解成正负离子,
在水中以分子形式存在,含有亲水基团和亲油基团。它有以下几类:酯类、醚类、胺类和酰胺类,典型代表是环氧乙烷聚合物,如R-(OC2H4)n-OH、RCO-(OC2H4)n-OH、R-C6H4-(OC2H4)n-OH 等,其中R=C10~C16,聚乙烯醇也属于这一类。这类乳化剂对pH 变化不敏感,但由于其乳化能力有限,在乳液聚合中不单独使用。
在实际的常规乳液聚合中,阴离子型乳化剂的共同特点是乳化效率高,能有效降低表面张力,用量可以较少,胶束和形成的乳胶粒子小,并由于其离子性质,使乳胶粒子带有电荷,对胶粒的分散稳定化是通过双电层作用实现的,使其对电解质和冻融过程,乃至对其他乳化剂品种均存在不同程度的敏感性,造成稳定性降低,容易起泡且难以消除。非离子型乳化剂以吸附保护作用使乳胶粒稳定,其特性与阴离子型恰恰相反,它对电解质的化学稳定性良好,但乳化能力弱,易在聚合过程中生成凝块,导致聚合速率减慢,乳胶粒径变大。正如以上所述,阴离子型乳化剂和非离子型乳化剂各有优缺点,将它们配合使用,取长补短,而且在两者复合使用时,两类乳化剂分子交替吸附在乳胶粒表面,即在离子型中嵌入非离子型,造成了一定的空间位阻,增大了乳化剂离子间的距离,减少了在同一乳胶粒上相邻乳化剂离子间的静电斥力,增加了阴离子乳化剂在乳胶粒上的吸附强度;另一方面,离子型乳化剂可以看成为电解质,非离子型乳化剂上的亲水基团与H2O 及H3O+ 通过氢键作用而带上正电荷,离子间发生静电作用,减少了亲水基团间的斥力,增加了乳化能力。因此,目前的常规乳液聚合多采用阴离子和非离子乳化剂的复配体系,从而提高了乳化剂的乳化作用,稳定了乳液聚合过程,制得的产物兼有粒径小、低泡、稳定的特点。但需要注意的是:乳化剂之间存在吸附竞争和空间位阻,影响体系的稳定性,当体系中乳胶粒子浓度较低时,体系的粘度小,粒子间的距离大,超出了电荷稳定和空间稳定的作用范围,在重力作用下容易发生沉降。
2.3 乳化剂的用量及配比
当少量乳化剂溶解于水中时,乳化剂以单个分子状态存在,导致水的表面张力以及界面张力急剧下降,但对单体仍不能起乳化增溶作用,不能形成稳定的水包油体系。只有当其浓度超过临界胶束浓度(CMC)时,乳化剂分子才能聚集在一起形成胶束,乳化增溶单体,形成增溶胶束,得到稳定的水包油系统,才能成为之后聚合反应的场所。不同乳化剂的CMC 值是不同的,对常规乳液聚合来说,CMC 值越小,乳化能力越强,CMC 值的大小还影响乳胶粒径的大小及分布。阴离子乳化剂CMC 值的大小由乳化剂结构,主要是疏水基团结构,及水中的电解质浓度决定。影响非离子乳化剂的主要因素则只是疏水基团的长度。乳化剂的用量不同,所形成的胶束浓度也不同。一般就常规乳液聚合而言,乳化剂用量在一定范围时,用量越大,体系中胶束浓度越大,形成的胶束多而且平均粒径小,粒径分布宽,有利于乳液聚合稳定。但乳化剂用量太大,导致体系粘度增大,难以搅拌,反应热难以散失,容易出现凝絮;粒径过小,界面能增大,耐电解质能力下降,并出现大量难以消除的泡沫,对乳液聚合以及整个乳液体系造成不良影响。若乳化剂浓度小,体系中乳化剂胶束浓度就低,仅部分乳胶粒表面被乳化剂分子覆盖,引发速度变慢,成核期变长,转化率低,粒径变大,粒径分布也同时变宽,如果乳化剂用量过小,乳液稳定性降低,乳胶粒也容易发生聚结,严重时会发生凝聚,造成挂胶和抱轴。因此要根据实验决定乳化剂的用量,通常来说,其用量是单体的2%~10%。
影响乳化剂乳化作用的另一个指标是乳化剂的亲油亲水平衡值(HLB 值)。每一种乳化剂都有某一特定的HLB 值,对大多数应用在常规乳液聚合的表面活性剂而言,其HLB 值在1~40 之间。HLB 值越低,表明其亲油性越大;HLB 值越高,则表明其亲水性越大。HLB 值影响乳液聚合速率,乳液的稳定性,乳液体系的粘度以及乳胶粒的大小。一般来说,常规的水包油型乳液聚合的HLB 值在8~18 之间,研究发现,当被乳化物与乳化剂的HLB 值相差很大时,乳化剂对被乳化物质的亲和力小,其乳化效果差;另一方面,乳化剂的HLB 值很小,则对水的亲和力小,乳化效果也差。若要达到较好的乳化效果,就要令两者的HLB 值相近,但这是任何一种乳化剂单独使用时都难以实现的,因此通常将两种或多种具有不同HLB 值的乳化剂混合成复合乳化剂,使性质不同的乳化剂由亲油到亲水之间过渡,就会大大增进乳化效果。一般常规乳液聚合的情况下,非离子型乳化剂比例较高或离子型与非离子型各半,但也要考虑实际情况,对机械稳定性不好的乳液加大阴离子乳化剂用量,可以减少搅拌片上吸附的凝聚物;对化学稳定性不好的乳液,增加非离子乳化剂的用量,可以减少反应容器内结皮等现象。
2.4 反应性乳化剂
以上所讲的常规乳液聚合的乳化剂都属于传统乳化剂,都不参与化学反应,通过调节它们的用量及配比等可令乳液聚合及产物稳定。但这些乳化剂都不能去除,会带到最终产品中,从而影响乳液聚合物的应用性能,如电性能、光学性能、表面性能及耐水性等。无皂乳液聚合因此备受关注,这种方法的其中一个实施手段是加入大量的亲水性单体,但同样会导致耐水性降低;另外一种实现方法是反应性乳化剂的使用。反应性乳化剂存在可以与单体进行共聚反应的双键,与单体共聚后永久键合到乳胶分子中,大大降低乳化剂分子从乳胶粒上解吸的倾向,乳化剂分子不会因迁移而导致乳胶凝聚,乳液成膜后乳化剂仍键合在粒子表面,不会向水中迁移,提高了膜层的耐水性,而且当反应性乳化剂用量适当时,可显著提高单体的反应活性,并且在水相中不存在乳化剂分子,加快了成膜速度。但反应性乳化剂的使用要注意与单体匹配,而且通常不单独使用。这与乳化剂的均聚能力与共聚能力有关,也就是竞聚率的问题,另一个原因是它的乳化能力,毕竟常规乳液聚合的目的是要得到性能良好的共聚物乳液,并且要有高的产率和转化率。只有当反应性乳化剂共聚能力和乳化能力均较强时才能够很容易地得到稳定的乳液,如果其自聚能力过强,在反应前期大部分就结合到分子链中,容易被包埋,反应后期就无足够的乳化剂包覆乳胶粒;如果仅有反应性乳化剂,那么体系就会失去稳定性,出现大量絮凝甚至破乳;但如果有传统乳化剂的存在,就可以继续起到乳化作用。若是反应性乳化剂的亲油链过短,对单体的亲和性不高,则乳化能力不强,易溶于水,形成均聚物,这时也需要传统乳化剂的参与调节乳化体系的亲水亲油平衡。所以反应性乳化剂通常与传统乳化剂共同使用,优势互补,大大降低传统乳化剂的用量及乳化剂的总用量,减少乳液聚合过程的泡沫,并能得到粒径小,化学稳定性和机械稳定性佳的乳液,成膜耐水性强。
3 引发剂
3 引发剂
引发剂对整个乳液聚合过程起着重要作用。用于乳液聚合的引发手段或引发剂很多,如超声辐照无引发剂引发、UV 光引发配合光引发剂(如异丙基硫杂蒽酮)引发、微波辐照配合引发剂(如偶氮二异丁基脒盐酸盐)引发、等离子体引发、纳米SiO2粒子锚固偶氮引发剂引发、油溶性引发剂引发。常规乳液聚合中一般采用水溶性引发剂:(1)能受热分解产生自由基的水溶性物质,如过硫酸钠盐、钾盐和铵盐以及较少使用的偶氮化合物;(2)由上述过硫酸盐和还原剂共同组成的氧化还原引发体系,常用的还原剂有亚硫酸氢盐、硫酸亚铁、硫醇,还有有机过氧化氢-亚铁盐氧化还原体系。不同的引发剂的引发效率和半衰期都不同,会对聚合反应及其产物造成不同的影响。通常引发剂的分解速率随温度的升高而增大,半衰期缩短,自由基生成浓度加大,从而影响乳液聚合反应及单体转化率。单独使用过硫酸盐作引发剂时,引发剂分解的活化能较高,引发温度高,聚合反应速率较低,聚合过程中容易失稳,产生絮凝,残余单体较多。但如果在热分解引发剂中加入还原剂,复配得到氧化还原引发剂,可以克服上述缺点。因为这两者产生自由基的机理是不同的,对于热分解引发剂来说,在热的作用下,分子中的原子可以获得很大的振动能量,当这些能量足以克服化学键能,分子就会均裂产生自由基;而氧化还原引发剂则是由这两个组分之间发生的氧化还原反应而产生自由基,改变了自由基的生成机理,大大降低了分解活化能,降低了引发温度。具体对比如表1 所示。

引发剂除了在种类方面影响乳液聚合以外,其浓度也严重影响乳液聚合。引发剂的用量影响其分解速率:引发剂浓度过低,产生的自由基少,体系中乳胶粒获得自由基的机率较小,诱导期长,参加聚合反应的有效乳胶粒数目少,聚合反应慢,最终转化率低,导致漂油,还会令乳胶粒子表面电位下降,致使粒径加大甚至相互聚结,乳液体系遭到破坏;增加引发剂的用量,水中自由基的有效生成速率增加,引发速度加快,成核速率和反应速率均提高,单体转化率提高,而且对于过硫酸盐引发体系来说,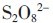 分解得到的HSO4- 会进一步解离得到H+ 和
分解得到的HSO4- 会进一步解离得到H+ 和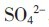 ,令体系pH 下降,提高引发剂分解速率,聚合物自由基硫酸根离子为亲水基团,带自由电子的一端为疏水基,使过硫酸盐又有类似于乳化剂的作用,提高乳液聚合的稳定性。但当引发剂用量过大时,体系中的自由基数目急剧增多,聚合速率迅速增大,体系粘度快速上升,成核粒子增多,反应热难以排出,温度容易波动,极易出现粗粒子,并产生大量氢离子,令体系pH 急剧降低,对乳化剂的乳化能力造成不良影响;而且引发剂属于电解质,用量太大使体系中电解质浓度过高,影响乳液聚合的稳定性,凝胶量进一步上升。在乳液聚合中,引发剂用量一般为单体的0.3%~1%,氧化剂与还原剂之比为1 ∶ 1。
,令体系pH 下降,提高引发剂分解速率,聚合物自由基硫酸根离子为亲水基团,带自由电子的一端为疏水基,使过硫酸盐又有类似于乳化剂的作用,提高乳液聚合的稳定性。但当引发剂用量过大时,体系中的自由基数目急剧增多,聚合速率迅速增大,体系粘度快速上升,成核粒子增多,反应热难以排出,温度容易波动,极易出现粗粒子,并产生大量氢离子,令体系pH 急剧降低,对乳化剂的乳化能力造成不良影响;而且引发剂属于电解质,用量太大使体系中电解质浓度过高,影响乳液聚合的稳定性,凝胶量进一步上升。在乳液聚合中,引发剂用量一般为单体的0.3%~1%,氧化剂与还原剂之比为1 ∶ 1。
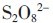 分解得到的HSO4- 会进一步解离得到H+ 和
分解得到的HSO4- 会进一步解离得到H+ 和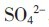 ,令体系pH 下降,提高引发剂分解速率,聚合物自由基硫酸根离子为亲水基团,带自由电子的一端为疏水基,使过硫酸盐又有类似于乳化剂的作用,提高乳液聚合的稳定性。但当引发剂用量过大时,体系中的自由基数目急剧增多,聚合速率迅速增大,体系粘度快速上升,成核粒子增多,反应热难以排出,温度容易波动,极易出现粗粒子,并产生大量氢离子,令体系pH 急剧降低,对乳化剂的乳化能力造成不良影响;而且引发剂属于电解质,用量太大使体系中电解质浓度过高,影响乳液聚合的稳定性,凝胶量进一步上升。在乳液聚合中,引发剂用量一般为单体的0.3%~1%,氧化剂与还原剂之比为1 ∶ 1。
,令体系pH 下降,提高引发剂分解速率,聚合物自由基硫酸根离子为亲水基团,带自由电子的一端为疏水基,使过硫酸盐又有类似于乳化剂的作用,提高乳液聚合的稳定性。但当引发剂用量过大时,体系中的自由基数目急剧增多,聚合速率迅速增大,体系粘度快速上升,成核粒子增多,反应热难以排出,温度容易波动,极易出现粗粒子,并产生大量氢离子,令体系pH 急剧降低,对乳化剂的乳化能力造成不良影响;而且引发剂属于电解质,用量太大使体系中电解质浓度过高,影响乳液聚合的稳定性,凝胶量进一步上升。在乳液聚合中,引发剂用量一般为单体的0.3%~1%,氧化剂与还原剂之比为1 ∶ 1。
4 其他因素
4.1 缓冲剂
正如以上所述,在常规乳液聚合反应中通常采用过硫酸盐作为引发剂,它的分解会产生氢离子,随着聚合反应的进行,体系中的氢离子浓度逐渐增大,这样就会加速引发剂的分解,反应不能以
平稳的速度进行,而且阴离子乳化剂对pH 敏感,只有在弱碱范围内有效,所以在聚合反应中常常添加缓冲剂,也称pH 调节剂。常用的缓冲剂有:NaHCO3、NH3·H2O、Na2HPO4、NaAc 和三乙胺等。缓冲剂也是体系中添加的主要电解质之一。一般来说,当电解质浓度低时,乳液聚合反应速率随着电解质浓度的增加而增加,乳液稳定性提高,当达到一定电解质浓度时,总的聚合反应速率达到最大值,乳液稳定性最佳;若此时再增加电解质浓度,聚合反应速率反而会降低,乳液失去稳定性,发生乳胶粒子的碰撞,造成絮凝。缓冲剂加入量过少,缓冲能力有限,不能保证体系pH 稳定,容易造成粒子凝聚,而且影响乳液的贮存稳定性;加入量过多,体系的离子强度增加过大,乳胶粒的双电层斥力变弱,ζ 电位降低,引发剂分解速率降低,单体转化率减少,乳胶粒径增大。只有适量地加入缓冲剂,通常为单体的0.3%~1.5%,才能有效地控制pH值并起到降低阴离子乳化剂CMC 值和加快引发剂分解速率的效果。
4.2 温度
辐射引发的引发温度较低,UV 光引发的引发温度也较低,常温即可进行。常规乳液聚合反应的最低温度必须保证在引发剂分解温度和混合乳化剂起乳化增溶作用的温度之上,以保证自由基能不断地产生并保证乳液体系的稳定,通常这个温度控制在反应的回流温度。温度过低,引发剂分解速率低甚至不能分解,乳化剂的乳化效率低,胶束数目减少,单体转化率低,凝胶严重;温度过高,引发剂分解速率过快,反应速率过高,聚合物粒子变软,粘性增加,乳液粒子布朗运动加剧,粒子间因碰撞而凝聚的可能性增大,容易出现粗粒子,聚合度降低。
4.3 搅拌速度
不同于某些乳液聚合可以在振荡下进行,常规乳液聚合是在连续搅拌下进行的。在乳化分散阶段,要求将单体分散成为小珠滴,进入胶束内部,形成大量粒径小的增溶胶束,搅拌强度不够,单体只能形成大珠滴,甚至分层,这一阶段要求较大的搅拌速率。在聚合反应进行时,应有中等的搅拌强度,过高会延长聚合的诱导期,过小则体系内部不能充分混合,单体容易在反应器上部形成一滞留层,乳化剂不能把单体充分乳化,单体不能充分被消耗,反应热不能及时散发,导致自动加速,最终反应器内会出现大量凝聚物。在反应后期,也要采用缓和的搅拌强度,过高会令乳液粒子激烈碰撞而凝聚,但也不能太低甚至不搅拌,这样会使乳液液面聚结成膜。
4.4 聚合工艺
4.4 聚合工艺
目前常规乳液聚合的基本工艺主要有一次投料法、半连续法和种子法。
一次投料法是将所有的单体、引发剂、乳化剂及所需物质一次投入到反应器中,然后升温至反应温度,开始反应,经历一段时间后降温出料。采用这种聚合方法,在反应经历了一段诱导期后,反应开始进行,一旦开始,由于热量大量产生,不能及时转移,会使反应器内部温度急剧升高,单体暴聚,并由于反应速率快,引发剂大量消耗,反应后期无足够的引发剂,乳化剂不能迅速地吸附到乳胶粒表面以维持乳胶粒的稳定,乳胶粒子之间的聚结作用力增大,从而导致凝聚使反应失稳。
半连续法是在一定温度下,先让部分单体在乳化剂溶液中经引发剂引发反应,进行到一定程度后,再将单体或单体预乳液不断滴加到反应器中,同时补加引发剂溶液,然后继续反应一定时间,达到一定转化率,降温出料。通过控制滴加速率,可使反应体系处于饥饿、半饥饿和充溢状态,则可获得结构不同,性能各异的聚合物乳液。令反应体系处于饥饿状态,加入的单体在乳胶粒表面聚合并增长,反应平稳进行,引发剂的不断加入保证了高转化率。
种子法是先制得种子乳液,然后再在种子基础上进一步进行聚合最终制得所需乳液。其工艺与半连续法相似,但可以通过改变种子单体和滴加单体的组成制得结构各异,性能更优的核壳乳液。
5 结语
人们在大量研究和生产实践中发现,乳液聚合体系具有粘度低、易散热、聚合反应速率高、产物相对分子质量大、所用设备和工艺简单等特点,且制得的聚合物乳液可以直接应用于很多领域,如将所得乳液用作涂料、粘胶剂、皮革、纸张、织物的处理和修饰等,所以到目前为止,常规乳液聚合已经发展成为高分子科学中一个非常活跃的研究领域和工业生产中不可或缺的部分。同时又因为这类体系是采用水为反应介质,成本低,对环境污染小,而且更符合人类可持续发展的要求,所以乳液聚合技术不但有强大的生命力,而且具有巨大的发展前景。






